2020년 알츠하이머 시장 규모 63억 달러…연평균 6.5% 성장 전망
펩타이드·줄기세포·항체 등 다양한 종류 및 기전 치료제 개발 활발
[메디코파마뉴스=박애자 기자] 전 세계적으로 알츠하이머 신약 개발이 활발하게 이뤄지고 있는 가운데 앞으로 국내 제약바이오기업들은 알츠하이머병 치료제 개발 목표를 ‘완화’의 개념이 아닌 명확한 원인 ‘치료’의 개념으로 변화해야 한다는 주장이 제기됐다.
한국바이오협회는 30일 ‘알츠하이머병의 진단과 치료제 개발 동향’ 보고서를 통해 국내외 임상개발 동향을 분석했다.
알츠하이머병은 치매를 일으키는 가장 흔한 퇴행성 뇌 질환으로, 국내 65세 이상 치매 환자 4명 중 3명은 알츠하이머형 치매로 알려져 있다.
글로벌 알츠하이머병 치료제 시장 규모는 2020년 63억 4,000만 달러에 달하며, 2021년부터 2026년까지 연평균성장률(CAGR) 6.5%로 확대될 것으로 예상되고 있다.
그러나 현재까지 미국식품의약국(FDA)에서 승인한 알츠하이머병 약물들은 인지기능을 개선하고 증상을 완화하는 목적 위주로 아직까지 근본적인 치료 약물이 없어 글로벌 시장의 미충족 수요가 매우 높은 상황이다.
현재까지 근본적인 치료제로 처음 허가를 받은 바이오젠의 ‘아두헬름(Aduhelm)’의 경우에도 임상 1상 (PRIME 연구)에서 경증 알츠하이머병 대상으로 아밀로이드 베타 제거에서의 안전성(Safety)과 효능(Efficacy)을 확인했지만 중증 알츠하이머병을 대상으로 한 임상 3상 시험에서는 충분한 유효성을 입증하지 못했다.
결국 임상 4상을 진행하는 조건으로 조건부 허가(가속화 승인, Accelerated Apporval)를 받았지만 이 또한 유효성 입증 서류 부족 사유로 지난 4월 20일 유럽의약품청(EMA) 승인 신청을 자진 철회했다.
그렇다면 현재 알츠하이머병 치료제 개발 현황은 어떻게 될까.
미국국립보건원이 운영하는 임상시험정보사이트(clinicaltrials.gov)의 2022년 알츠하이머병 신약 임상 상황에 따르면, 2021년 전 세계에서 143개 신약 후보물질을 대상으로 총 172건의 임상시험이 시행됐다.
상용화에 가장 근접한 임상 3상에 진입한 신약 후보물질은 31개(임상 47건)로, 임상 2상 82개(임상 94건), 임상 1상은 30개(임상 31건) 순이었다.
세부적으로 원인조절치료제(Disease-modifying therapy, DMT)는 143개의 전체 후보물질 중 119개(83.2%)로 대부분을 차지했다.
지난해 신약 임상에서도 DMT의 경우 126개 전체 후보물질 가운데 104개로 82.5%의 높은 점유율을 보인만큼, 해당 용도의 후보물질은 꾸준히 큰 비중을 차지하고 있는 것으로 확인됐다.
다음으로 인지기능 강화제(Cognitive enhancer) 14개(9.8%), 신경정신행동 증상 개선제(Neuropsychiatric and behavioral)가 10개(6.9%)로 나타났다.
원인조절치료제(DMT)의 종류는 바이오의약품 40개(33.6%), 저분자 의약품 79개(66.4%)로 구분됐으며, 원인조절치료제(DMT) 용도의 후보물질 임상은 아밀로이드 베타 표적 계열이 20개(16.8%), 타우 단백질 표적 계열이 13개(10.9%)였다.
상용화를 타깃으로 하는 임상 3상 현황의 경우 31개의 약물에 총 47건의 임상이 진행됐으며, 알츠하이머병 치료에 대한 약물이 용도별로 다양하게 분포됐다.
원인조절치료제(DMT) 임상이 67.8%로 대부분이었으며, 증상조절제(Neuropsychiatric Symptom)가 16%, 인지증진약물(cognitive enhancers)이 16%를 차지했다.
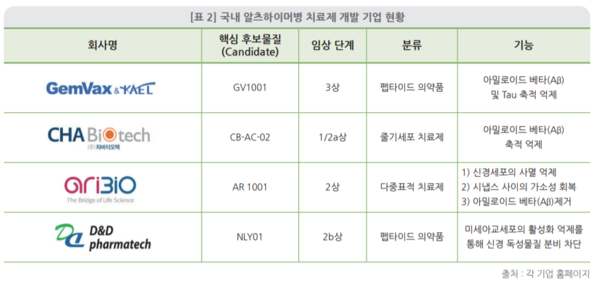
≫ 국내 제약바이오 기업도 알츠하이머병 치료제 개발 활발
국내 제약바이오 기업 역시 줄기세포치료제, 펩타이드 의약품 등 알츠하이머병 치료제 개발에 활발한 편이다.
현재 국내에서 알츠하이머병 치료제를 개발하는 곳은 젬백스앤카엘, 차바이오텍, 아리바이오, 디앤파마텍, 에이비엘바이오 등이다.
젬백스앤카엘은 지난 1월 식품의약품안전처로부터 중증 알츠하이머병 환자를 대상으로 펩타이드의약품 ‘GV1001’ 3상 임상시험을 승인받았다. 젬백스앤카엘은 GV1001의 신경세포 보호 효과를 통해 알츠하이머병 치료 효능을 확인할 수 있을 것으로 보고 있다.
차바이오텍은 줄기세포 치료제 기반의 알츠하이머병 치료제를 개발 중이다. ‘신경 전구세포(neuronal progenitor cell)’ 배양 기술을 개발한 차바이오텍은 대량 증식한 신경 전구세포가 신경세포로 분화하도록 유도해 알츠하이머병, 헌팅턴병 등 신경질환 치료에 이용할 수 있을 것으로 기대하고 있다.
아리바이오는 단일 기전 약물에 집중해 온 다국적 제약사들과는 다르게 약물 하나로 여러 작용을 하는 ‘다중기작’ 약물을 개발 중이다.
항체 치료제를 개발하는 곳도 있다. 에이비엘바이오는 뇌혈관장벽(BBB) 셔틀 플랫폼인 ‘그랩바디-B’를 활용해 퇴행성뇌질환 치료제 ‘ABL301’을 연구하고 있다.
디앤디파마텍은 퇴행성 뇌신경질환 신약 후보물질 'NLY01'을 개발하고 있다. 지난 2020년 미국 식품의약국(FDA)으로부터 알츠하이머성 치매 2b상을 승인받은 상태다.
이 밖에도 셀트리온과 아이큐어가 공동개발을 통해 알츠하이머병 치매 치료용 도네페질 패치제에 대한 식약처 품목허가를 획득했다.
이 외 다른 기업들은 경구제나 주사제 이외에도 다양한 제형의 임상 및 상용화를 진행하고 있다.
바이오협회는 “알츠하이머병 치료제 개발의 경우 성공률이 매우 낮고 최근 임상 3상에서 실패하는 경우가 다수 발생하지만 치료제 시장을 빠르게 선점하기 위해 전 세계적으로 2022년 기준 170여 개의 글로벌 파이프라인을 통한 연구가 진행 중”이라며 “신약 개발에 대한 성공 확률이 낮은 만큼 정부의 적극적인 지원 및 민간 기업의 수요에 대응하기 위한 장기적인 전략과 투자가 중요하다”고 말했다.
그러면서 “알츠하이머병 치료제 개발 현황 중 원인조절치료제(DMT)의 연구가 가장 많다는 사실에 비춰 볼 때 전세계적으로 알츠하이머병의 근원적인 치료를 위한 방법을 모색하고 있다는 것을 시사한다”며 “앞으로 알츠하이머병 치료제는 ‘완화’의 개념이 아닌 명확한 원인 ‘치료’의 개념으로 변화해야 한다”고 제언했다.

